18 Ekim 2024’te, ABD Gıda ve İlaç İdaresi (FDA), Astellas Pharma tarafından geliştirilen zolbetuximab-clzb (Vyloy) adlı ilacı, CLDN18.2 pozitif tümörleri olan, ameliyat edilemeyen veya metastatik HER2-negatif mide ya da gastroözofageal bileşke (GEJ) adenokarsinomu olan yetişkin hastaların tedavisinde ilk basamak tedavi olarak onayladı (kaynak).
Bu ilaç, floropirimidin ve platin bazlı kemoterapi ile birlikte kullanılacak. Aynı zamanda FDA, zolbetuximab ile tedaviye uygun hastaları belirlemek için VENTANA CLDN18 (43-14A) RxDx Tanı Testi’ni de onayladı.
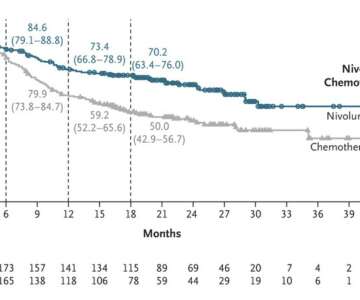
İlacın etkinliği, SPOTLIGHT ve GLOW adlı iki klinik çalışmaya dayandırıldı. Bu çalışmalarda zolbetuximab, kemoterapi ile birlikte kullanıldığında hastaların hastalık ilerleme sürelerini (PFS) ve genel sağkalımlarını (OS) plasebo grubuna kıyasla anlamlı ölçüde artırdı.
• SPOTLIGHT çalışmasında, zolbetuximab grubunda medyan PFS 10,6 ay, OS ise 18,2 ay olarak bulundu. Plasebo grubunda ise PFS 8,7 ay, OS 15,5 ay olarak ölçüldü.
• GLOW çalışmasında, zolbetuximab grubunda medyan PFS 8,2 ay, OS ise 14,4 ay olarak bulunurken, plasebo grubunda bu süreler sırasıyla 6,8 ve 12,2 ay idi.